■ 무선 초음파 스캐너 ‘SonoMe’ 유럽 의료기기 인허가 승인
■ 소노미, 유럽연합(EU)의 엄격한 의료기기 인증 규정 확보
■ “인허가 리스크 해소하며 유럽지역 내 사업 확장 계획”
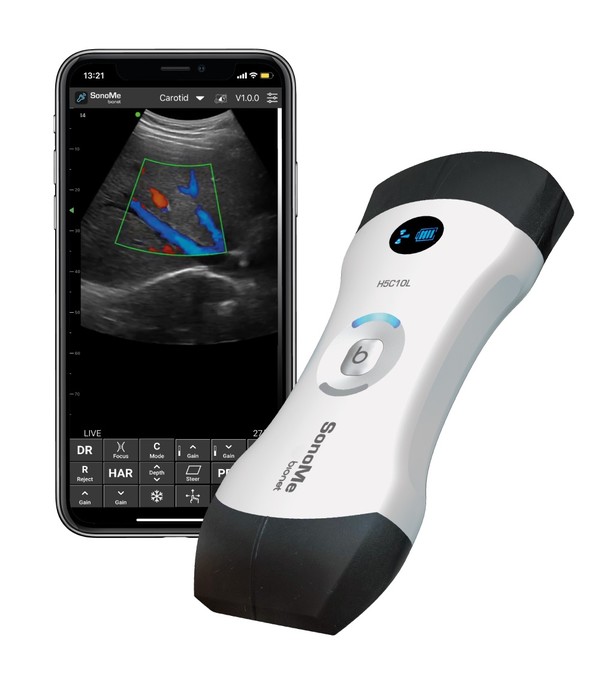
의료기기 제조사 바이오넷(대표이사 라종주)이 지난 25일 무선 이동형 초음파 스캐너 ‘소노미’의 CE MDR 인증을 획득했다고 30일 밝혔다.
CE MDR(Medical Device Regulation)은 CE(Conformite Europeenne)가 1993년에 만든 의료기기 지침(MDD, Medical Device Directive)의 품질과 안전기준을 높여 2017년에 새롭게 법제화 되었다.
유럽연합(EU) 지역으로 수출되는 모든 의료기기에 필수로 요구되는 인증 규정으로 2021년 5월부터 시행되고 있으며, 기존 CE MDD 인증보다 엄격한 평가 절차와 관리·통제·사후 감시 등을 통해 제품 안정성과 품질시스템을 확보하여 신뢰성을 증대하고 있다.
바이오넷은 이러한 규정을 충족시키기 위해 엄격한 품질 관리 및 테스트 절차를 거쳤으며, 그 결과 국내 최초로 무선 이동형 초음파 스캐너 제품에 대한 CE MDR 인증을 받았다.
이번에 인증받은 제품인 ‘소노미’는 의료용 초음파 영상 진단장치로 지난 2021년 국내 식품의약품안전처(MFDS)에 이어, 2022년 미국 식품의약청(FDA) 인허가를 획득한 제품이다. 모바일 장비에 와이파이로 연결하는 무선 프로브 제품이며 휴대가 용이해 다양한 임상 환경에서 초음파 진단이 가능한 것이 특징이다.
바이오넷의 라종주 대표는 “국내 무선 초음파 의료기기 제조사 중 최초로 CE MDR 인증을 획득했다는 점에서 큰 의미가 있다. 인허가 리스크가 해소된 만큼 유럽지역에 소노미 제품 수출을 더욱 적극적으로 추진하여 수출 경쟁력을 강화하겠다”라고 전했다.
한편, 바이오넷은 오는 11월 13일부터 16일까지 독일에서 개최되는 세계 최대 의료기기 전시회 ‘MEDICA 2023’에 참가하여 유럽 시장 진출에 박차를 가할 예정이다.

